-
摘要: 针对局部分割方法对初始轮廓敏感的问题,本文提出一种基于模糊主动轮廓的鲁棒局部分割方法.该方法利用图像的局部信息,定义一种新的平均模糊能量函数.通过对演化曲线进行形态学膨胀和腐蚀运算构建窄带,并在窄带范围内求解模糊能量函数的最小值来实现局部分割.为防止演化曲线陷入局部极小值,在迭代过程中加入对比度约束判断条件,进一步提高了分割方法对初始轮廓的鲁棒性.对合成图像和医学图像的分割实验结果表明,与已有的几种局部分割方法相比,本文方法在分割精度和鲁棒性等方面都有较大提高.Abstract: Since the local segmentation method is sometimes sensitive to the initial contour, a robust local segmentation method based on average fuzzy-energy based active contour is proposed in this paper. A new average fuzzy energy function is defined by using the local image information. In order to achieve local segmentation, the minimization of energy function is solved in a narrow band constructed by morphological dilation and erosion operations. A contrast constraint condition is added in the iterative process to prevent the curve from falling into local minimum, which can further improve the robustness of the segmentation model against initial contour. Experimental results on synthetic images and medical images show that, compared to several existing local segmentation methods, the proposed method has considerable improvement in segmentation accuracy and robustness.
-
Key words:
- Fuzzy clustering /
- active contour /
- local segmentation /
- membership /
- contrast constraint
-
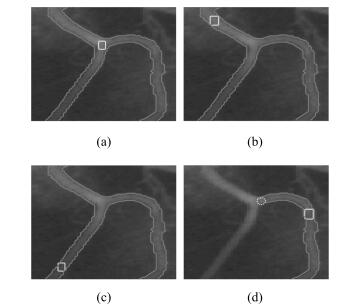
图 5 图 4 (d) 中伪边缘区域像素点的灰度值、隶属度、均值差及 $\beta$ = 1:8时分割结果
Fig. 5 The intensity, membership and difierence of pixels near the pseudo edge in Fig. 4 (d) and segmentation result when $\beta$ = 1:8
-
[1] Kass M, Witkin A, Terzopoulos D. Snakes:active contour models. International Journal of Computer Vision, 1988, 1(4):321-331 doi: 10.1007/BF00133570 [2] Malladi R, Sethian J A, Vemuri B C. Shape modeling with front propagation:a level set approach. IEEE Transactions on Pattern Analysis and Machine Intelligence, 1995, 17(2):158-175 doi: 10.1109/34.368173 [3] Caselles V, Kimmel R, Sapiro G. Geodesic active contours. International Journal of Computer Vision, 1997, 22(1):61-79 doi: 10.1023/A:1007979827043 [4] Chan T F, Vese L A. Active contour without edges. IEEE Transactions on Image Processing, 2001, 10(2):266-277 doi: 10.1109/83.902291 [5] Vese L A, Chan T F. A multiphase level set framework for image segmentation using the Mumford and Shah model. International Journal of Computer Vision, 2002, 50(3):271-293 doi: 10.1023/A:1020874308076 [6] Li C M, Kao C Y, Gore J C, Ding Z H. Implicit active contours driven by local binary fitting energy. IEEE Conference on Computer Vision and Pattern Recognition, 2007, 2007(1):1-7 http://citeseerx.ist.psu.edu/viewdoc/summary?doi=10.1.1.140.9182 [7] Bezdek J C, Ehrlich R, Full W. FCM:The fuzzy c-means clustering algorithm. Computers and Geosciences, 1984, 10(2-3):191-203 doi: 10.1016/0098-3004(84)90020-7 [8] Chen Z, Qui T, Ruan S. Fuzzy adaptive level set algorithm for brain tissue segmentation. In:Proceedings of the 9th International Conference on Signal Processing, Beijing, China:IEEE, 2008. 1047-1050 [9] Li B N, Chui C K, Chang S, Ong S H. Integrating spatial fuzzy clustering with level set methods for automated medical image segmentation. Computers in Biology and Medicine, 2011, 41(1):1-10 doi: 10.1016/j.compbiomed.2010.10.007 [10] Chuang K S, Tzeng H L, Chen S, Wu J, Chen T J. Fuzzy c-means clustering with spatial information for image segmentation. Computerized Medical Imaging and Graphics, 2006, 30(1):9-15 doi: 10.1016/j.compmedimag.2005.10.001 [11] Li C, Xu C, Gui C, Fox M D. Level set evolution without re-initialization:a new variational formulation. In:Proceedings of the 2005 IEEE Computer Society Conference on Computer Vision and Pattern Recognition, San Diego, USA:IEEE, 2005. 430-436 [12] Alipour S, Shanbehzadeh J. Fast automatic medical image segmentation based on spatial kernel fuzzy c-means on level set method. Machine Vision and Applications, 2014, 25(6):1469-1488 doi: 10.1007/s00138-014-0606-5 [13] Zhang D Q, Chen S C. A novel kernelized fuzzy c-means algorithm with application in medical image segmentation. Artificial Intelligence in Medicine, 2004, 32(1):37-50 doi: 10.1016/j.artmed.2004.01.012 [14] Shi Y, Karl W C. A real-time algorithm for the approximation of level set based curve evolution. IEEE Transactions on Image Process, 2008, 17(5):645-656 doi: 10.1109/TIP.2008.920737 [15] Rastgarpour M, Shanbehzadeh J, Soltanian-Zadeh H. A hybrid method based on fuzzy clustering and local region-based level set for segmentation of inhomogeneous medical images. Journal of Medical Systems, 2014, 38(8):1-15 [16] Krinidis S, Chtzis V. A robust fuzzy local information c-means clustering algorithm. IEEE Transactions on Image Processing, 2010, 19(5):1328-1337 doi: 10.1109/TIP.2010.2040763 [17] Li C M, Huang R, Ding Z H, Gatenby J C, Metaxas D N, Gore J C. A level set method for image segmentation in the presence of intensity inhomogeneities with application to MRI image processing. IEEE Transactions on Image Processing, 2011, 20(7):2007-2016 doi: 10.1109/TIP.2011.2146190 [18] Samson C, Blanc-Feraud L, Aubert G, Zerubis J. A level set model for image classification. International Journal of Computer Vision, 2000, 40(3):187-197 doi: 10.1023/A:1008183109594 [19] 谢振平, 王士同.融合模糊聚类的Mumford-Shah模型.电子学报, 2008, 36(1):127-132 http://www.cnki.com.cn/Article/CJFDTOTAL-DZXU200801023.htmXie Zhen-Ping, Wang Shi-Tong. An extended Mumford-Shah model integrated with fuzzy clustering. Acta Electronica Sinica, 2008, 36(1):127-132 http://www.cnki.com.cn/Article/CJFDTOTAL-DZXU200801023.htm [20] Krinidis S, Chatzis V. Fuzzy energy-based active contour. IEEE Transactions on Image Processing, 2009, 18(12):2747-2755 doi: 10.1109/TIP.2009.2030468 [21] Shyu K K, Pham V T, Tran T T, Lee P L. Global and local fuzzy energy-based active contours for image segmentation. Nonlinear Dynamics, 2012, 67(2):1559-1578 doi: 10.1007/s11071-011-0088-1 [22] 唐利明, 王洪珂, 陈照辉, 黄大荣.基于变分水平集的图像模糊聚类分割.软件学报, 2014, 25(7):1570-1582 http://www.cnki.com.cn/Article/CJFDTOTAL-RJXB201407015.htmTang Li-Ming, Wang Hong-Ke, Chen Zhao-Hui, Huang Da-Rong. Image fuzzy clustering segmentation based on variational level set. Journal of Software, 2014, 25(7):1570-1582 http://www.cnki.com.cn/Article/CJFDTOTAL-RJXB201407015.htm [23] Ahmed M N, Yamany S M, Nevin M, Farag A A, Thomas M. A modified fuzzy c-means algorithm for bias field estimation and segmentation of MRI data. IEEE Transactions on Medical Imaging, 2002, 21(3):193-199 doi: 10.1109/42.996338 [24] 唐利明, 田学全, 黄大荣, 王晓峰.结合FCMS与变分水平集的图像分割模型.自动化学报, 2014, 40(6):1233-1248 http://www.aas.net.cn/CN/abstract/abstract18394.shtmlTang Li-Ming, Tian Xue-Quan, Huang Da-Rong, Wang Xiao-Feng. Image segmentation model combined with FCMS and variational level set. Acta Automatica Sinica, 2014, 40(6):1233-1248 http://www.aas.net.cn/CN/abstract/abstract18394.shtml [25] Thieu Q T, Luong M, Rocchisani J M, Sirakov N M, Viennet E. Efficient segmentation with the convex local-global fuzzy Gaussian distribution active contour for medical applications. Annals of Mathematics and Artificial Intelligence, 2015, 75(1):249-266 http://dl.acm.org/citation.cfm?id=2825798 [26] Shi J, Zhou Y, Lei Y. A narrow band interval type-2 fuzzy approach for image segmentation. Journal of Systems Architecture, 2015, 64:86-99 https://www.researchgate.net/publication/284123480_A_Narrow_Band_Interval_Type-2_Fuzzy_Approach_for_Image_Segmentation [27] 陈侃, 李彬, 田联房.基于模糊速度函数的活动轮廓模型的肺结节分割.自动化学报, 2013, 39(8):1257-1264 http://www.aas.net.cn/CN/abstract/abstract18157.shtmlChen Kan, Li Bin, Tian Lian-Fang. A segmentation algorithm of pulmonary nodules using active contour model based on fuzzy speed function. Acta Automatica Sinica, 2013, 39(8):1257-1264 http://www.aas.net.cn/CN/abstract/abstract18157.shtml [28] 张迎春, 郭禾.基于粗糙集和新能量公式的水平集图像分割.自动化学报, 2015, 41(11):1913-1925 http://www.aas.net.cn/CN/abstract/abstract18766.shtmlZhang Ying-Chun, Guo He. Level set image segmentation based on rough set and new energy formula. Acta Automatica Sinica, 2015, 41(11):1913-1925 http://www.aas.net.cn/CN/abstract/abstract18766.shtml [29] Lankton S, Tannenbaum A. Localizing region-based active contours. IEEE Transactions on Image Processing, 2008, 17(11):2029-2039 doi: 10.1109/TIP.2008.2004611 [30] Mille J. Narrow band region-based active contours and surfaces for 2D and 3D segmentation. Computer Vision and Image Understanding, 2009, 113(9):946-965 doi: 10.1016/j.cviu.2009.05.002 [31] Zhang K H, Song H, Zhou W. Active contours with selective local or global segmentation:a new formulation and level set method. Image and Vision Computing, 2010, 28(4):668-676 doi: 10.1016/j.imavis.2009.10.009 [32] 郑强, 董恩清.一种新的基于二值水平集和形态学的局部分割方法.电子与信息学报, 2012, 34(2):375-381 http://www.cnki.com.cn/Article/CJFDTOTAL-DZYX201202021.htmZheng Qiang, Dong En-Qing. A new local segmentation method based on binary level set and morphological operation. Journal of Electronics and Information Technology, 2012, 34(2):375-381 http://www.cnki.com.cn/Article/CJFDTOTAL-DZYX201202021.htm [33] Zheng Q, Dong E Q. New local segmentation model for images with intensity inhomogeneity. Optical Engineering, 2012, 51(3):037006-1-037006-10 http://opticalengineering.spiedigitallibrary.org/pdfaccess.ashx?url=/data/journals/optice/24207/oe_51_3_037006.pdf&resultclick=1 [34] 郑强, 董恩清.窄带主动轮廓模型及在医学和纹理图像局部分割中的应用.自动化学报, 2013, 39(1):21-30 http://www.aas.net.cn/CN/abstract/abstract17809.shtmlZheng Qiang, Dong En-Qing. Narrow band active contour model for local segmentation of medical and texture images. Acta Automatica Sinica, 2013, 39(1):21-30 http://www.aas.net.cn/CN/abstract/abstract17809.shtml [35] Zheng Q, Dong E Q, Cao Z L, Sun W Y, Li Z G. Modified localized graph cuts based active contour model for local segmentation with surrounding nearby clutter and intensity inhomogeneity. Signal Processing, 2013, 93(4):961-966 doi: 10.1016/j.sigpro.2012.10.005 [36] Zheng Q, Dong E Q, Cao Z L, Sun W Y, Li Z G. Active contour model driven by linear speed function for local segmentation with robust initialization and applications in MR brain images. Signal Processing, 2014, 97(7):117-133 https://www.researchgate.net/publication/259098934_Active_contour_model_driven_by_linear_speed_function_for_local_segmentation_with_robust_initialization_and_applications_in_MR_brain_images [37] Dong E Q, Zheng Q, Sun W Y, Li Z G, Li L. Constrained multiplicative graph cuts based active contour model for magnetic resonance brain image series segmentation. Signal Processing, 2014, 104(6):59-69 https://www.researchgate.net/publication/261918774_Constrained_multiplicative_graph_cuts_based_active_contour_model_for_magnetic_resonance_brain_image_series_segmentation [38] Bai X J, Li C M, Sun Q S, Xia D S. Contrast constrained local binary fitting for image segmentation. In:Proceedings of the 2009 International Symposium on Visual Computing, Las Vegas, NV, USA:Springer Berlin Heidelberg, 2009. 886-895 [39] Li X L, Chen X J, Yao J H, Zhang X, Yang F, Tian J. Automatic renal cortex segmentation using implicit shape registration and novel multiple surfaces graph search. IEEE Transactions on Medical Imaging, 2012, 31(10):1849-1860 doi: 10.1109/TMI.2012.2203922 -




 下载:
下载: